Schützende Substanzen gegen Zelltod im Gehirn von Parkinson-Patienten
Forschungsleitung: Prof. Dr. Günter Höglinger
Studie: Validierung von chemischen Verbindungen aus einem Hochdurchsatz-Screening zur Identifikation von neuen Molekülen, die gegen alpha-Synuclein induzierte Toxizität schützen
Dauer: 3 Jahre
Ziel der 3-jährigen Studie
Das Ziel der Studie ist es, eine Leitsubstanz zu ermitteln, welche die Entwicklung zukünftiger neuroprotektiver Medikamente ermöglichen, die den Zelltod im Gehirn von Parkinson-Patienten und damit den Krankheitsverlauf verlangsamen oder gar verhindern werden.
Der ParkinsonFonds Deutschland hat bereits das erfolgreiche Vorgängerprojekt gefördert, bei dem nach Substanzen gesucht wurde, die den Zelltod, welcher bei Morbus Parkinson auftritt, verhindern können. Nach einem Hochdurchsatz-Screening von 50.000 Substanzen wurden 232 Substanzen gefunden, die von ihren Eigenschaften her geeignet wären, humane, dopaminerge Neurone gegen von alpha-Synuclein induzierten Zelltod zu schützen.
Die neue und potenziell revolutionäre Studie geht einen Schritt weiter:
In einem mehrstufigen Verfahren werden von den 232 Substanzen diejenigen herausgefiltert, die mit größter Effizienz gegen den durch alpha-Synuclein vermittelten Zelltod schützen. Zudem soll deren Struktur hinsichtlich Struktur-Wirkungsbeziehung analysiert werden, um solche Strukturmotive zu identifizieren, die für den Schutz vor alpha-Synuclein vermittelter Toxizität verantwortlich sind. Durch Analyse von Struktur-Wirkungsbeziehungen erhoffen sich die Wissenschaftler, eine Grundstruktur zu finden, die als Gerüst für einen neuen Wirkstoff zur krankheitsmodifizierenden Therapie bei der Parkinson-Krankheit in Frage kommt.
Dies könnte den Weg für die Entwicklung eines Medikaments bereiten, welches Parkinson verhindern oder den Krankheitsverlauf verlangsamen wird.
Das Ziel der Studie wird erreicht, indem
- Substanzen untersucht werden, die in Zellkultur schon zeigten, dass sie gegen den Alpha-Synuclein vermittelten Zelltod schützen konnten.
- erforscht wird, warum dabei manche Substanzen effektiver waren als andere.
- der Wirkmechanismus der effektiven Substanzen entschlüsselt wird.
Unter dem Mikroskop auch für das bloße Auge sichtbar
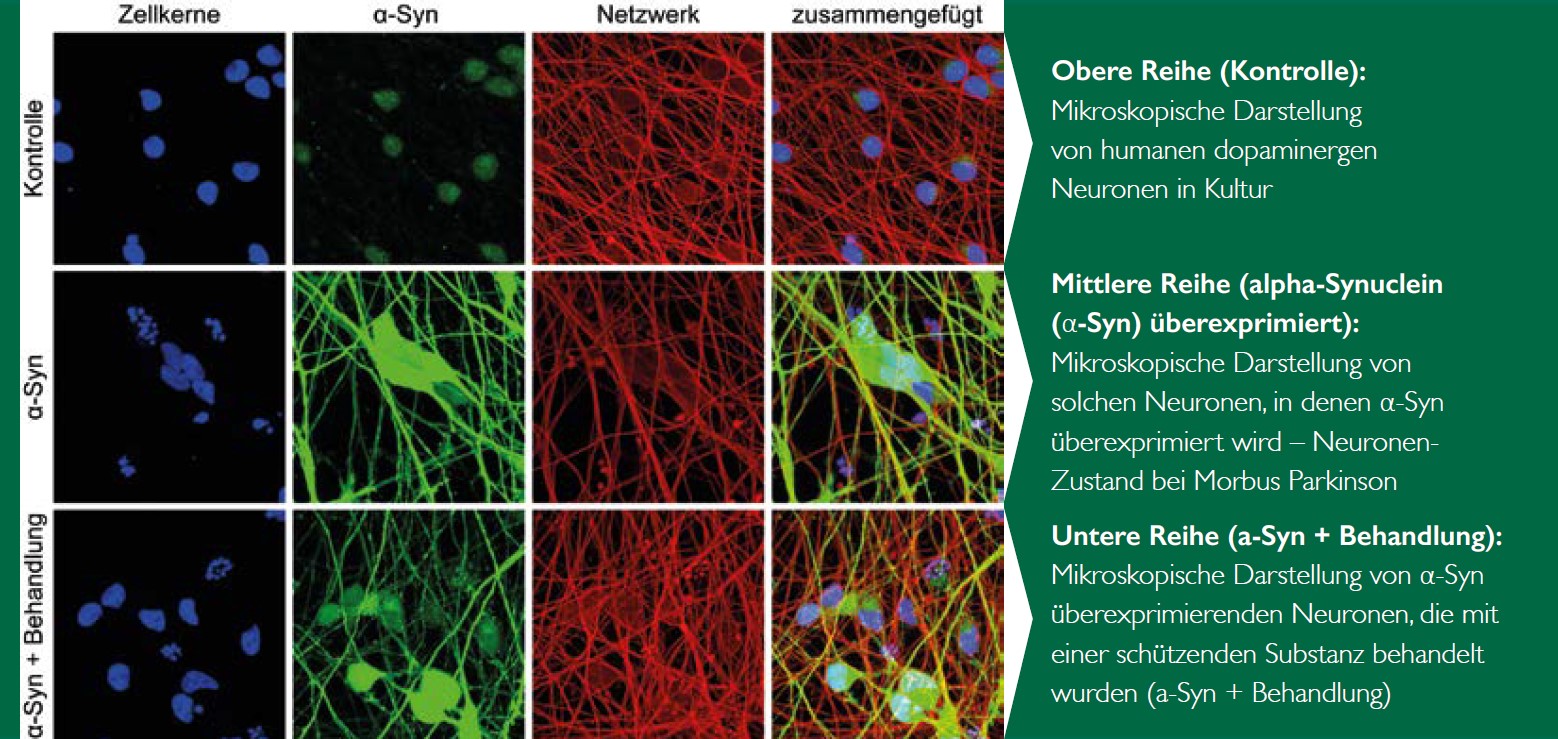
Wird die Zelle mit einer schützenden Substanz behandelt, kann
- der Zellkern geschützt werden, was man daran sieht, dass unter Behandlung mehr Kerne sichtbar sind (in blau, linke Spalte, untere Reihe),
- die Integrität des neuronalen Netzwerks (in rot, dritte Spalte, untere Reihe) erhalten bleiben.
Aus diesen Gründen unterstützt der ParkinsonFonds Deutschland diese Forschung
- Die Studie ist zukunftsweisend und potenziell revolutionär.
Es handelt sich um eine grundlagenwissenschaftliche Arbeit zur Entwicklung zukünftiger Therapien, die den Zelltod im Gehirn von Patienten verlangsamen oder gar verhindern sollen. - Die Förderung der Studie ist die konsequente Fortsetzung der bisherigen erfolgreichen Zusammenarbeit.
Der ParkinsonFonds Deutschland hat bereits das Vorgängerprojekt gefördert, in dem gezeigt werden konnte, dass die Durchführung von Hochdurchsatz-Screenings zur Identifikation neuer möglicher neuroprotektiver Therapieansätze bei der Parkinson-Krankheit im akademischen Umfeld erfolgreich möglich ist. - Die Bedingungen sind optimal.
Renommierte junge Wissenschaftler widmen sich an den anerkannten Standorten München und Dresden einer einzigartigen besonders aussichtsreichen Studie. Die Forschung von Prof. Höglinger und Dr. Höllerhage wurde deshalb von unserem medizinisch-wissenschaftlichen Beirat als besonders förderungswürdig eingestuft. - Die Entwicklung neuer Therapieansätze, um Zellen vor dem Zelltod zu schützen, ist von größter Brisanz und Bedeutung.
Zum gegenwärtigen Zeitpunkt existiert kein Medikament, das den Zelltod einzelner Zellen im Gehirn von Patienten mit einer Parkinson-Krankheit verhindern und damit den Krankheitsverlauf verlangsamen kann.
Das Team hoch motivierter Wissenschaftler
Prof. Dr. Günter Höglinger

Prof. Dr. Günter Höglinger
Prof. Höglinger studierte Medizin und Physik an den Universitäten Regensburg und Würzburg. Im Jahr 2000 promovierte er im Fach Humanmedizin (summa cum laude). Mit einem DFGStipendium ging er als Postdoc an das Hôpital de la Salpêtrière, Paris. Seit 2004 leitete er die Arbeitsgruppe für Experimentelle Neurologie der Philipps-Universität Marburg. Dort absolvierte er auch die Ausbildung zum Facharzt für Neurologie und arbeitete abschließend als leitender Oberarzt. Seit 2011 hat der Wissenschaftler einen Lehrstuhl für Translationale Neurodegeneration am Deutsches Zentrum für Neurodegenerative Erkrankungen (DZNE) inne und ist Oberarzt in der Neurologischen Klinik der Technischen Universität München.
Seine wichtigsten Auszeichnungen: Dingebauer-Preis der Deutschen Gesellschaft für Neurologie (2017), Heisenberg-Professur der Deutschen Forschungsgemeinschaft (2011), Award for Excellence der Movement Disorders Society (2007) und der Forschungspreis der Deutschen Parkinson Vereinigung (2005).
Dr. med. Matthias Höllerhage

Dr. med. Matthias Höllerhage
Ko-Leiter der Studie
Federführend wird insbesondere der Ko-Leiter Dr. Höllerhage für das Projekt verantwortlich sein. Er absolvierte sein Medizinstudium an der Philipps-Universität in Marburg und promovierte im Fach Humanmedizin (2010, summa cum laude). Seit 2012 arbeitet der Wissenschaftler in der Neurologischen Klinik und Poliklinik des Klinikums rechts der Isar der Technischen Universität München. 2017 erhielt Dr. Höllerhage die Anerkennung als Facharzt für Neurologie.
Seine wichtigste Auszeichnung: Wissenschaftspreis der Deutschen Parkinson-Gesellschaft 2017.
„Das bessere Verständnis der Mechanismen, die zum Zelltod bestimmter Zellen im Gehirn von Patienten mit einer Parkinson-Krankheit führen, und insbesondere das Verständnis von Möglichkeiten, dies zu verhindern, kann für zukünftige Patientengenerationen sehr nützlich sein, weil diese zur Entwicklung von neuroprotektiven Medikamenten beitragen werden.“ – Dr. med. Matthias Höllerhage
Ablauf und Kosten der Studie
Wie gestaltet sich der Ablauf der Studie?
- Zunächst werden die 232 Substanzen hinsichtlich Struktur-Wirkungsbeziehung im Computer analysiert.
- Dann werden 60 Substanzen anhand ihrer chemischen Struktur und ihrer Effektivität im Primärscreening ausgewählt.
- Nach dieser Analyse werden 40 Substanzen mit möglichst hoher chemischer Diversität selektiert.
- Nun werden wiederum die 20 vielversprechendsten Substanzen selektiert und hinsichtlich ihres Wirkmechanismus analysiert.
- Abschließend soll eine Leitstruktur bzw. eine Leitsubstanz identifiziert werden, und die zu einem Medikament zur krankheitsmodifizierenden Therapie für Morbus Parkinson entwickelt werden könnte.
Wie setzen sich die Kosten der Studie zusammen?
In erster Linie entstehen Personalkosten für einen betreuenden Wissenschaftler (Senior Scientist) sowie eine Doktorandin oder einen Doktoranden. Bei der Durchführung der Zellkulturexperimente werden Geldmittel benötigt für Verbrauchsmittel wie Zellkulturplatten, Zellmedien und Wachstumsfaktoren. Im Rahmen der Studie wird eine automatisierte bildgebende Analyse der Feinstruktur des neuronalen Netzwerks durchgeführt. Um dieses sichtbar zu machen, werden Antikörper benötigt. Des Weiteren entstehen Kosten für die automatisierte Bildaquisition und -analyse. Auch müssen vielversprechende Substanzen neu synthetisiert werden, was ebenfalls Kosten verursacht.
EINE EINZIGARTIGE STUDIE, DIE ES UNBEDINGT ZU FINANZIEREN GILT
“Der Krankheitsverlauf von Parkinson könnte verzögert oder sogar gestoppt werden. Die Auswirkungen dieser Entwicklung könnte die Parkinson-Forschung revolutionieren!
Da die Studie langfristig angelegt ist, werden Personen, die sich aktuell im Frühstadium der Parkinson-Krankheit befinden, und Personen, die mit einem großen Risiko behaftet sind, später an Parkinson zu erkranken, vom erfolgreichen Abschluss der Studie profitieren können. Ich hoffe, Sie erkennen das zukunftsweisende Potenzial dieser Forschung. Ihr Entschluss, die Studie finanziell zu fördern, wird die Forschung nach einer wirksamen Parkinson-Therapie einen
bedeutenden Schritt voranbringen.“
Lassen Sie uns gemeinsam diese wichtige Studie realisieren und die Zukunft der Parkinson-Therapie revolutionieren
„Im Namen der aktuell und künftig Betroffenen danke ich Ihnen aufrichtig für Ihren wertvollen Beitrag zur Parkinson-Forschung.”
– Prof. Dr. Günter Höglinger

 Spenden
Spenden